![]()
試薬
・微小管固定バッファー(MTSB)
作り方:
1. 1.50 g PIPES, 0.19 g EGTA, 0.13 g MgSO4 7H2Oおよび0.50 g KOHを800 mlの蒸留水に溶かす。
2. KOHを使ってpHを7.0に調整する。
3. 蒸留水により液量を1000 mlに調整する。
・3% (w/v) パラフォルムアルデヒド in MTSB(4℃保存。実験には調整後1週間以内のものを用いる。廃液は、フォルマリン廃液として処理する。)
作り方:
1. 10 mlのMTSBを80℃に温める。
2. 0.3 g パラフォルムアルデヒドを加え、沸騰しないように溶かす(湯煎が望ましい。ドラフト内で行う)。
・10 x PBS緩衝液
作り方:
1. 80 g NaCl, 2 g KCl, 35.8 g Na2HPO4 12H2Oおよび2.4 g KOHを800 mlの蒸留水に溶かす。
2. HClを使ってpHを7.4に調整する。
3. 蒸留水により液量を1000 mlに調整する。
・PBS緩衝液
作り方:
1. 10 x PBS緩衝液を蒸留水で10倍希釈する。
・5% (w/v) 低融点寒天 in PBS buffer
作り方:
1. 0.5 g 低融点寒天を10 mlのPBS緩衝液に溶かす。
・ 0.1% (w/v) pectolyase and 0.3% (v/v) Triton X-100 in PBS
作り方:
1. 10 mg Pectolyase Y-23(盛進製薬)を10 mlのPBS緩衝液に溶かす。
2. 30 μlのTriton X-100を加える。
・5% (w/v) BSA in PBS
作り方:
1. 0.5 g BSAを10 mlのPBS緩衝液に溶かす。
・1次抗体反応液(保存不可)
作り方:
1. 目的の1次抗体を適切な濃度になるように、1穴あたり150 μlのPBS緩衝液に加える (適正濃度が不明な場合は、1/100希釈から試してみる)。
・2次抗体反応液(保存不可)
作り方:
1. 2次抗体を適切な濃度になるように、1穴あたり150 μlのPBS緩衝液に加える。 (Alexa Fluor抗体の場合は1/300〜3000希釈が良い)。
器具
・Microslicer (LinearSlicer PRO10; Dosaka EM)
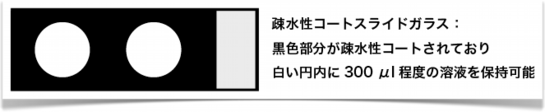
・ 疎水性コートスライドガラス(MATSUNAMI SF17380等)
・22 x 22 mmカバーガラス
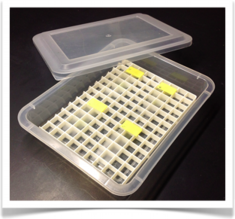
・湿箱(プラスチック容器にスノコを入れたもの。写真参照)
実験操作(Yamaji & Ma 2007を改変)
1. 2 cm程度に切断した根端を 3% (w/v) パラフォルムアルデヒド in MTSB中、室温で20分間固定する。
2. 溶液を取り除き(フォルマリン廃液として処理すること)、PBS緩衝液で10分間ずつ2回洗浄する。
3. シャーレ中、40℃の5% (w/v) 低融点寒天 in PBS bufferに根を沈め包埋する。
4. 4℃で寒天を硬化させる。
5. Microslicer (LinearSlicer PRO10; Dosaka EM)を用いて、厚さ100 μmの切片を切り出す。
6. 疎水性コートスライドガラスの上に保持したPBS緩衝液中に切り出した切片を浮かべる。
7. PBS緩衝液を取り除き、150 μlの0.1% (w/v) pectolyase and 0.3% (v/v) Triton X-100 in PBSを加える。
8. スライドを湿箱中、30℃で2時間保温する。
9. 酵素液を取り除き、300 μlのPBS緩衝液により洗浄する(3回)。
10. 150 μlの5% (w/v) BSA in PBSを加え、室温で10分間ブロッキングする。
11. ブロッキング液を取り除き、150 μlの1次抗体を含むPBS緩衝液を加える。
12. スライドを湿箱中、室温で一晩保温する。
13.1次抗体液を取り除き、300 μlのPBS緩衝液により洗浄する(3回)。
14. 150 μlの5% (w/v) BSA in PBSを加え、室温で10分間ブロッキングする。
15. ブロッキング液を取り除き、150 μlの2次抗体を含むPBS緩衝液を加える。
16. スライドを湿箱中、室温で2時間保温する。
17. 2次抗体液を取り除き、DNA染色色素(0.1 μg/ml DAPI等)を含むPBS緩衝液 300 μl により10分間染色する。
18. 染色液を取り除き、300 μlのPBS緩衝液により洗浄する(3回)。
19. 10 μlの退色防止剤を加え、22 x 22 mm カバーガラスをかぶせる。
20. カバーガラスの4辺とスライドガラス間の隙間をマニュキアにより封印する。
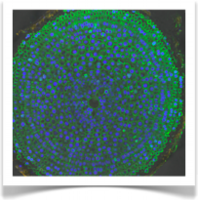
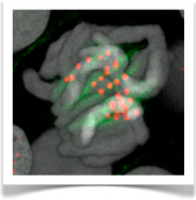
21. 共焦点レーザー顕微鏡により観察する。
 iPad用iBooks版はこちら
iPad用iBooks版はこちら

 蛍光免疫染色〜研究室...
蛍光免疫染色〜研究室...